广州海关:如何区分医用和民用口罩
海关总署关于印发
《海关实施出口医疗物资法定检验工作方案》的通知》
(署监发「2020」72号)
内容摘要及解读如下:
按照72号文件要求,对于53号公告规定的11类(19个商品编码)出口法检医疗物资,采取的是验证管理方式,就是不需要做商品品质检验,无需出口电子底账,企业正常申报报关单。
单证提交要求:在三部委发布的“5号公告”里的5类医疗物资,提交医疗器械产品注册证和企业承诺声明;在三部委发布的“5号公告”外的医用物资,企业提交注册证和质量安全承诺书,非医用物资不要求提交注册证和质量安全承诺书。
海关审核要求:三部委5号公告涉及5类医疗物资,而海关53号公告涉及11类医疗物资。其中,4类相同,7类不相同。但都是对于医疗物资的新措施,不是对于非医疗物资的新措施。所以,海关申报系统中并没有对53号公告中的19个HS设置出口商检监管条件。海关采取电子审核加人工审单的方法,处理53号文件涉及的申报单证。涉及53号公告的出口防疫物资申报时,不需要电子底账,数据不走ECIQ系统。三部委5号公告的4类商品按5号公告要求办理,需提供中国医疗器械产品注册证和企业承诺说明书,不需要做产品法定检验。对53号公告新增的7类商品,综合业务岗位几乎100%人工审单,发现未放行的可以联系海关审单部门。对非医用的,若没被布控,直接放行;对医用的,需企业提供注册证书(可以是电子扫描件)及出口企业的质量承诺书,有上传的,原则上(被风险布控或者综合业务岗人工审单有疑问的、决定布控除外)予以放行,没有上述注册证书或者出口企业质量保证承诺书的,将可能被布控。
查验资料要求:如果产品涉及医疗物资,企业需提供注册/备案证明和质量安全承诺书。对于现场无法判定或企业提出异议的送实验室检测。72号文中明确了“在确定是否为医疗物资时,应根据商品本身特征而非申报用途”。
近期,国外新冠肺炎持续爆发,对口罩等防疫物质需求大增,由于各国标准不同,我国出口非医用口罩误作医用的情况时有发生。3月31日,商务部会同海关总署、药监局发布《关于有序开展医疗物资出口的公告》(2020年第5号),要求出口医用口罩等5类产品必须取得国家药品监管部门相关资质,符合进口国(地区)质量标准要求。
那么,究竟如何快速准确地区分医用与非医用口罩呢?请跟发布君一起来了解
口罩的基本分类与细分
口罩从用途可以分为医用/非医用两大类。顾名思义,医用口罩主要用于医疗方面的防护,可以细分为医用防护、医用外科、一次性医用三种;非医用口罩也被称为个人防护口罩,可根据其适用场景,可细分为防颗粒物和日常防护两种。不同用途的口罩其技术要求不同、适用范围也不同。
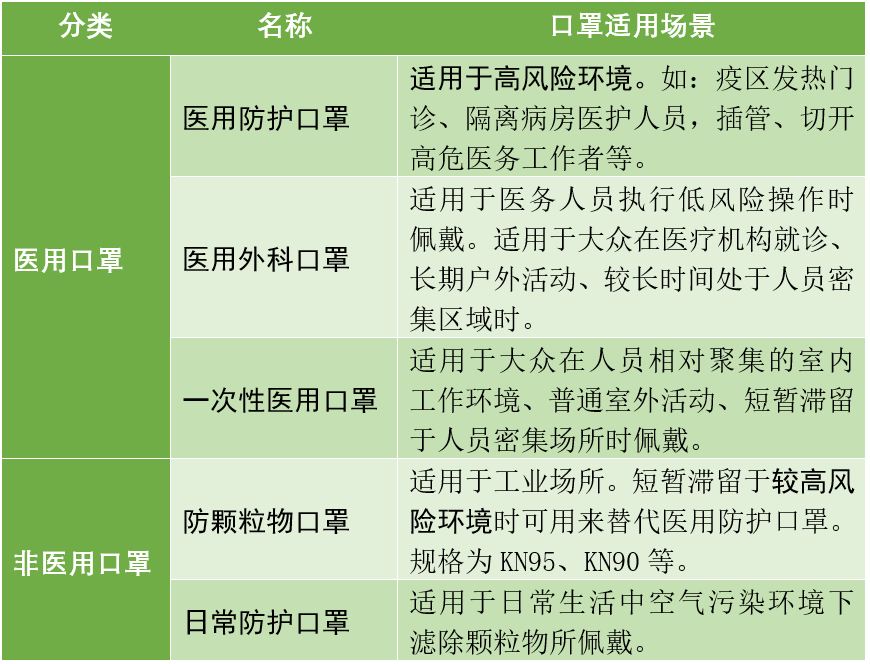
利用外观与包装信息区分医用/非医用口罩
通过口罩结构区分
通过过滤阀分辨。带过滤阀的口罩一般不会是医用口罩。如中国医用防护口罩标准GB 19803-2010 第4.3条款就明确规定“口罩不应有呼气阀”,这样可避免飞沫、微生物等通过呼气阀呼出,从而危害他人。而民用口罩允许有呼气阀,通过呼气阀可以减小呼气阻力,从而有利于作业人员长时间工作。
正规途径销售的口罩产品的最小单元包装上应该有商品名称、执行的标准和防护等级等信息。这些商家明示的信息可以作为一个分辨点,如商品名称中带有“医用”或英文“surgical”“Medical”等字样的,一般可判定为医用口罩。

适用标准区分医用/非医用口罩
医用口罩在不同国家/地区适用不同的标准和认证要求,企业和个人可根据产品进口国家/地区,根据产品的适用标准进行区分,产品适用标准和认证信息可从产品外包装或生产者提供的检测报告或证书获得。
医用口罩在美国属于医疗器械,适用《医用口罩材料性能标准规范》(ASTM F2100),由美国食品药品监督管理局(FDA)管理,须通过501K注册或近期FDA公布的其它途径,获得工厂注册和医疗器械列名后方可在美国上市。因此,输往美国的口罩外包装或检测报告或证书上有上述内容的,可被判定为医用口罩。
出口美国非医用口罩不属2020年第5号公告范围,但企业应注意,产品需通过NIOSH注册方可在美国上市。

欧盟医用/非医用口罩均需加贴CE标志,但适用标准不同。
医用口罩在欧盟属于I类器械,分为I类非无菌和无菌两种,需按照欧盟医疗器械指令93/42/EEC(MDD)或欧盟医疗器械条例EU2017/745(MDR)加贴CE标志,对应的标准是EN14683,输往欧盟的口罩外包装或检测报告、证书上有上述内容的,可被判定为医用口罩。
需要注意的是,根据口罩无菌/非无菌状态,欧盟采取不同的合格评定办法,非无菌医用口罩企业只需进行CE自我符合性声明,不需要通过公告机构认证。在准备好相应文件及测试报告等资料后,即可自行完成符合性声明。无菌医用口罩还必须由授权公告机构进行CE认证。
出口欧盟非医用口罩不属于医疗器械,但需符合欧盟个人防护设备条例EU2016/425(PPE)要求,由授权公告机构进行CE认证并颁发证书,对应的标准是EN149。
输往其它国家和地区口罩产品,可参考其提供的中国标准检测证书与注册备案信息进行判断,中国医用口罩标准有三个,GB 19083-2010、YY 0469-2011、YY/T 0969-2013,使用这三个标准生产的口罩可被判定为医用口罩。
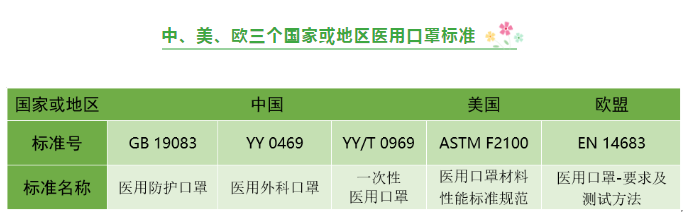
通过政府注册管控信息进行区分
由于医用口罩在大部分国家或地区都是按照医疗器械进行注册或管控的,消费者可以进一步通过相关注册管控信息进行分辨。下面以中、美、欧三个国家和地区举例分析。
医用口罩在中国属于二类医疗器械,是由省一级药品监管部门实施注册管理,可以通过医疗器械查询医疗器械准入号进行查询。链接为:
http://www.nmpa.gov.cn/WS04/CL2590/。
已获得美国FDA准入的口罩产品可以通过其官网查询注册证书号进行查询,链接为:
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfPMN/pmn.cfm
另外根据FDA最新政策,目前是在满足一定条件的情况下认可中国标准的口罩,其授权企业的链接为:
https://www.fda.gov/media/136663/download。
出口欧盟医用口罩可通过获得授权的公告机构进行查询,其中欧盟医疗器械指令93/42/EEC(MDD)授权的公告机构查询地址为:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13。
欧盟医疗器械条例EU 2017/745(MDR)授权的公告机构查询地址为:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34。
海关总署商检司将不定期更新部分国家或地区防疫物资技术法规和标准,目前已更新至第三版,点击“阅读原文”了解更多哦!链接为:
http://sjs.customs.gov.cn/sjs/zcfg56/2951967/index.html
供稿/ 广州海关
审核/ 海关总署商品检验司
监制/ 陶永
审校/ 刘畅
编辑/ 李灵
美术编辑/ 卫昊



