4月1日起医疗物资出口有新规!附CE/FDA认证资格认证指南
美国突然取消对中国KN95口罩标准认可!
28日,美国食品药品管理局(FDA)又推出了一个新的“紧急使用管理”(Emergency-Use-Administration,简称EUA),声明可以满足指定性能标准的可接受的口罩标准只有六个国家和地区,两周前还被认可的中国口罩标准消在名单中失了!

公告地址:
3月28日,美国FDA更新了Non-NIOSH批准口罩的紧急使用许可EUA。在这份发布的文件中,明确提到:其他国家提供的呼吸器产品,使用与NIOSH相似的一些方法对这些产品进行了评估。根据美国FDA已发布指导意见,中国的KN95口罩不再获准在美国使用。该指南将中国排除在Non-NIOSH的国家名单之外。包括KN95、KP100、KN100和KP95中国制造的口罩都将不在EUA名单之列。
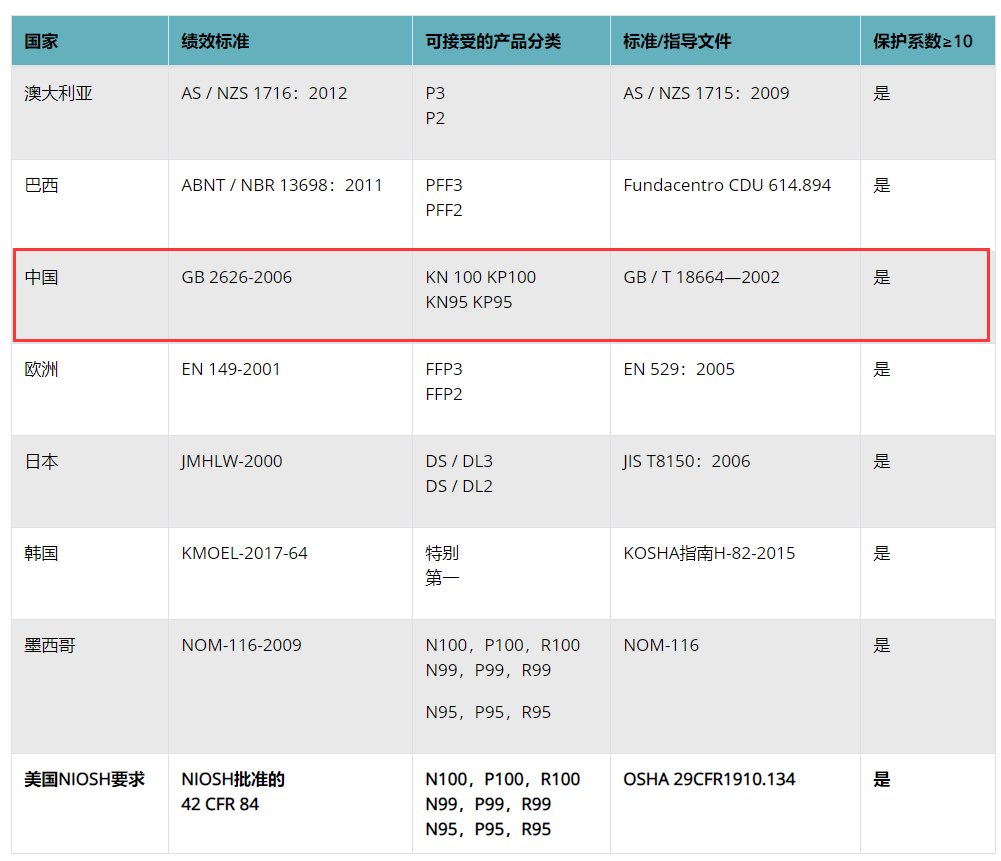
而此两周前的3月17日,美国疾控中心(CDC)公布了“优化N95呼吸器供应的策略:危机/替代策略”,批准了其它国家与N95同级别的口罩可以在美国替代使用,名单中包含巴西、韩国、日本、澳大利亚、欧洲、墨西哥和中国(含国内的四个口罩型号:KN100, KP100, KN95, KP95),共七个国家和地区。之前还宣称接受中国口罩标准的FDA,为何仅仅两周之后,就正式通知消失了呢?而且,对比先后两个通知,美国之外7个拟被认可标准的国家名单中,唯独缺少中国!
根据公告,当NIOSH意识到假冒口罩或在市场上歪曲NIOSH批准的口罩时,美国CDC发布了一批虚假口罩名单,以提醒用户、购买者和制造商。
商务部:4月1日起!出口医疗物资出新规
当前全球疫情形势严峻,为了满足国内疫情防控需要的基础上,鼓励企业扩大产能,有序出口,为国际社会抗击疫情提供力所能及的帮助,根据中央应对新冠肺炎疫情工作领导小组部署,商务部会同相关部门建立工作机制,对相关医疗物资进行严格的质量把控,严厉打击假冒伪劣行为。
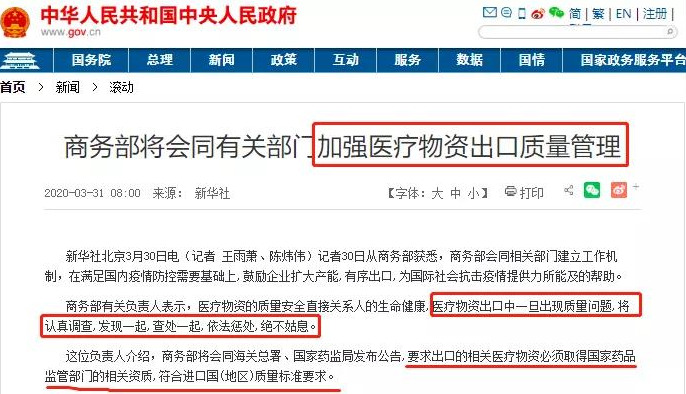
根据商务部与海关总署、药监局联合发布的公告,出口的相关医疗物资必须取得国家药品监管部门的相关资质,符合进口国(地区)质量标准要求。同时,也希望外国采购商选择符合上述质量要求的产品供应商。医疗物资出口中一旦出现质量问题,将认真调查,发现一起,查处一起,依法惩处,绝不姑息。目前,包括阿里巴巴和MIC在内的跨境电商平台将暂停上传中国医疗用品,直到供应商提交医用产品的相关资质或经营许可,这些产品才能重新上线。
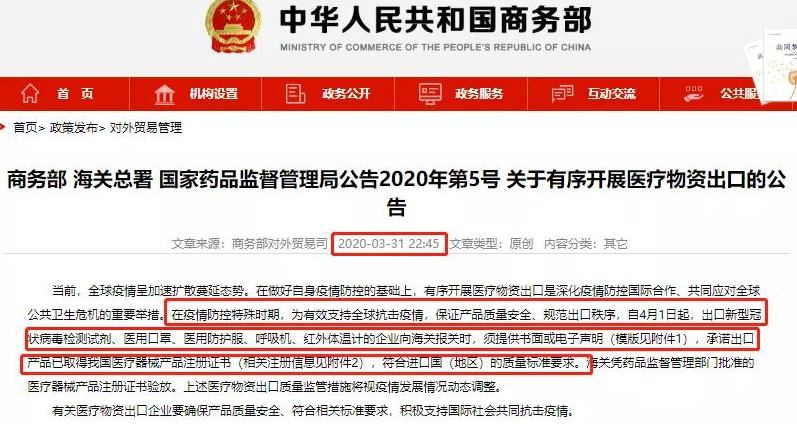
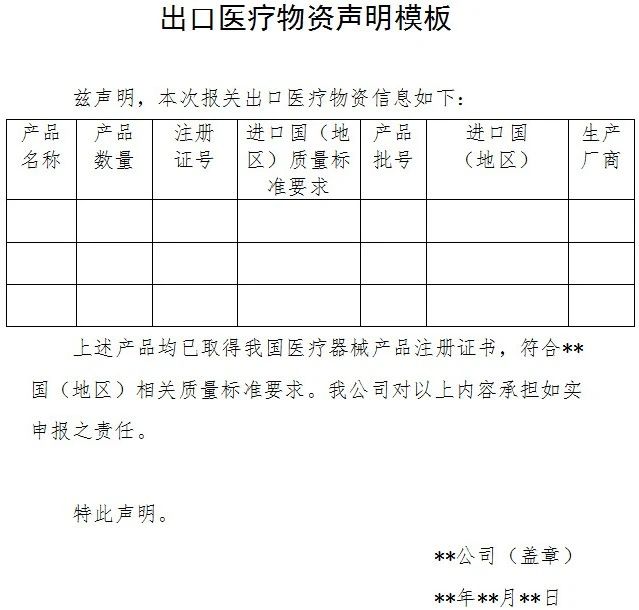
商务部昨晚发布公告:在疫情防控特殊时期,为有效支持全球抗击疫情,保证产品质量安全、规范出口秩序,自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明(模版见附件1),承诺出口产品已取得我国医疗器械产品注册证书(相关注册信息见附件2),符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。上述医疗物资出口质量监管措施将视疫情发展情况动态调整。